Азитромицин спасает детей, но вызывает устойчивость бактерий
Представьте себе: в бедных регионах Африки детям дважды в год дают антибиотик азитромицин. Это спасает тысячи жизней — смертность среди малышей снижается на 13-18%. Но учёные давно бьют тревогу: массовое применение антибиотиков может привести к появлению устойчивых бактерий. Что перевесит — польза или риск?
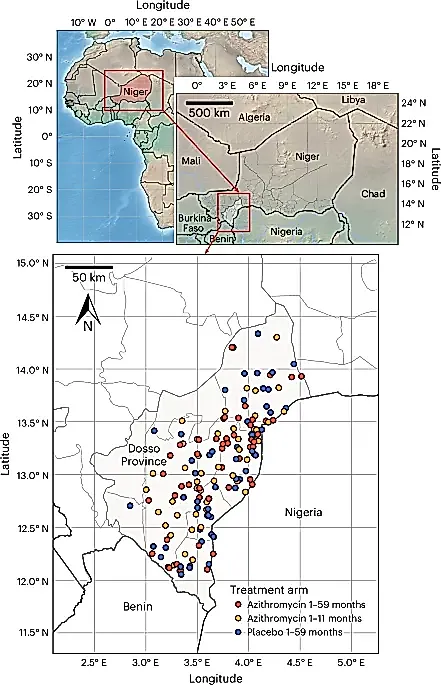
Недавно в журнале Nature Medicine вышло большое исследование под названиемAVENIR (Azithromycine pour la Vie des Enfants au Niger). Учёные изUniversity of California, San Francisco и их коллеги из Нигера проверили, как массовые раздачи азитромицина влияют на устойчивость бактерий в кишечнике и носоглотке детей.
Как проходило исследование
В эксперименте участвовали 3000 сельских общин в Нигере. Их разделили на три группы:
- Детская группа: азитромицин получали все дети от 1 месяца до 5 лет.
- Группа младенцев: антибиотик давали только малышам до года (1-11 месяцев), а детям постарше — плацебо (пустышку).
- Контрольная группа: все дети получали плацебо.
Лечение проводили раз в полгода в течение двух лет. Затем учёные взяли анализы у 4382 детей — мазки из кишечника и носоглотки, чтобы посмотреть, какие бактерии там живут и насколько они устойчивы к антибиотикам.
Что нашли в кишечнике
Главный результат: в кишечнике детей, которые получали азитромицин, бактерии стали более устойчивыми к макролидам (это класс антибиотиков, к которому относится азитромицин).
- В детской группе устойчивость былана 16% выше, чем в контрольной группе. Разница статистически значимая.
- В группе младенцев особого роста устойчивости не заметили — всего на 4% по сравнению с плацебо, и это не считается существенным.
- Интересно, что когда сравнивали две группы с азитромицином, то в детской группе устойчивость была на 13% выше, чем в группе младенцев.Почему это важно? Устойчивость в основном связана с геномermF. Представьте его как «ключ», который бактерии используют, чтобы заблокировать действие антибиотика. Этот ген чаще всего находят у бактерийBacteroides иPrevotella — обычных обитателей нашего кишечника, которые иногда могут вызывать инфекции.
Хорошая новость: к другим классам антибиотиков (например, пенициллинам) устойчивость не увеличилась.
А что в носоглотке?
Тут картина другая. Учёные не обнаружили значимого роста устойчивости к макролидам в носоглотке ни в одной из групп.
Хотя цифры показывали увеличение в 2 раза в группах с азитромицином, разброс данных был слишком большим, чтобы считать это доказанным эффектом. Не нашли и изменений в конкретных генах устойчивости, характерных для пневмококка (основной возбудитель пневмонии).
Но кое-что изменилось: в носоглотке детей, получавших азитромицин, стало больше бактерий Porphyromonas gingivalis иPrevotella intermedia — они связаны с заболеваниями дёсен и тоже могут нести гены устойчивости.
Микробиом остался прежним
Учёные проверили, не нарушает ли азитромицин общий баланс микрофлоры. Оказалось, что разнообразие бактерий в кишечнике и носоглотке не изменилось через полгода после последней дозы. Структура микробиома осталась похожей во всех группах.
Это обнадёживает — антибиотик не вызвал дисбактериоз в долгосрочной перспективе. Но некоторые конкретные виды бактерий (те самые Bacteroides и Prevotella) стали встречаться чаще.
Что это значит для нас?
Исследование AVENIR подтвердило, что массовые раздачи азитромицина действительноповышают устойчивость бактерий в кишечнике, особенно когда антибиотик получают все дети до 5 лет. Но этот эффект оказалсяскромнее, чем ожидали — всего 16% против 200-700% в более ранних работах.
Почему так? Учёные предполагают несколько причин:
- В регионе уже была высокая фоновая устойчивость из-за широкого использования антибиотиков.
- Программы профилактики малярии, которые тоже включают антибиотики, могли «замаскировать» эффект.
- Устойчивые бактерии могли передаваться между общинами, смазывая картину.Главный вывод: польза от снижения детской смертности пока перевешивает риски. Номониторинг устойчивости бактерий должен стать обязательной частью таких программ. Как сказал один из авторов,Thomas M. Lietman, нужно тщательно следить за балансом между спасением жизней сегодня и потенциальными проблемами завтра.
Исследование также показывает, что важно проверять устойчивость не только культуральными методами (выращивание бактерий в лаборатории), но и генетическими тестами. Некоторые устойчивые бактерии, как Bacteroides, плохо растут в обычных условиях, и их можно «поймать» только по ДНК.Что дальше? Учёные продолжают наблюдение в рамках проектаAVENIR II. Они хотят понять, как устойчивость влияет на реальные заболевания и не будет ли долгосрочных последствий для здоровья детей, получавших антибиотик. Аналогичные программы сейчас запускаются в Мали и Нигерии — там тоже будут внимательно следить за устойчивостью бактерий.
Для нас, обычных людей, это исследование — напоминание: антибиотики всегда палка о двух концах. Они спасают жизни, но их неконтролируемое применение ведёт к появлению супербактерий. Даже в критически важных программах, как в Африке, нужно находить баланс и постоянно отслеживать последствия.